Günümüzde BioNTech ile ortak geliştirdiği koronavirüs aşısıyla bilinen dünyanın en büyük ilaç şirketlerinden birisi olan Pfizer, oldukça önemli bir haberle yeniden gündeme geldi. COVID-19’a karşı hap şeklinde ilaç geliştiren şirket, Amerika Birleşik Devletleri’nin ardından Avrupa Birliği’nin ilaç düzenleyicisinden yeşil ışık almayı başardı.
Avrupa Birliği’nin ilaç düzenleyicisi Avrupa İlaç Ajansı (EMA), paylaştığı duyuruda Pfizer tarafından geliştirilen ‘Paxlovid’ adlı antiviral ilacın koşullu pazar onayı almasının önerildiği açıklandı. Paxlovid, alacağı bu onayla birlikte AB’de COVID-19 tedavisinde ağızdan alınarak kullanılan ilk onaylanmış ilaç olacak.
Oksijen tedavisine ihtiyacı olmayan hastalarda kullanılabilecek
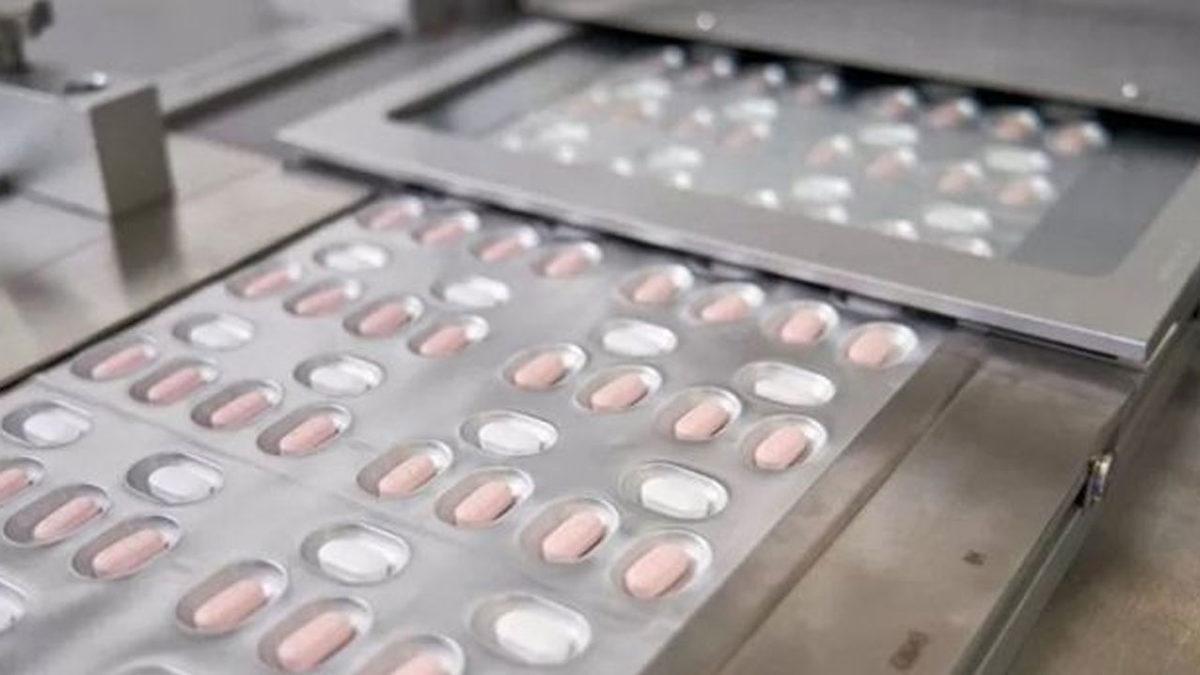
Pfizer tarafından EMA’ya yapılan Paxlovid başvurusu, ilacın 12 yaşından büyük hastaların tedavisi için yapılmıştı. Ancak EMA, ilacın ‘oksijen tedavisine gereksinimi olmayan ve hastalığın şiddetli hale gelme riski olan’ yetişkin hastalarda kullanılabileceğini kaydetti. İlacın COVID-19’un delta varyantına karşı etki gösterdiği, Omicron ve diğer varyantlara karşı da etkili olmasının beklendiği belirtildi.
Geçtiğimiz aralık ayında ABD Gıda ve İlaç İdaresi’nden acil kullanım onayı alan ilaç, Pfizer’in açıklamalarına göre hastaneye yatış ve ölümü engelleme konusunda %88 oranında başarı sağlıyor. Hollanda İlaç Değerlendirme Kurulu Başkanı Ton de Boer’in açıklamalarına göre ilaç, kısa süreli tat değişikliği, baş ağrısı, kusma ve kan basıncında geçici artış gibi hafif yan etkilere neden olabiliyor. Paxlovid ilacı, PF-07321332 ve ritonavir içeren iki farklı haptan oluşuyor.
Avrupa Komisyonu, bu yeşil ışıkla birlikte Paxlovid için şartlı pazar izni hakkında bir karar vermek üzere karar sürecini hızlandıracak ve sonunda bu ilacın AB genelinde pazarlanmasına izin verecek. Onay verildikten sonra şirketler, ilacın faydalarının risklerden daha ağır basmaya devam ettiğini doğrulamak için önceden tanımlanmış son tarihlere kadar daha fazla veri sunacak.










 Paylaş
Paylaş





 0
0